A_Neurobiology_015_ChemicalControl
Chemical Control of the Brain and Behavior
Introduction
中枢神经系统的通信并不止于瞬时、局部、点对点(Point-to-point)的突触传递。谷氨酸(Glutamate)与 GABA 介导的快速信号构成了神经网络计算的基础,但当行为需要被塑造为一种“状态”(state)——例如持续的警觉、睡眠、压力、饥渴、性动机或情绪背景——大脑往往依赖更慢、更弥散、覆盖更广的化学控制机制。这些机制可以被理解为在更大的空间与时间尺度上运行的三类输出:其一是 Secretory Hypothalamus (分泌性下丘脑) 通过血液分泌激素,改变全身的“体液背景(hormonal soup)”;其二是 Autonomic Nervous System (ANS, 自主神经系统) 以双神经元通路接管内脏与腺体;其三是 Diffuse Modulatory Systems (弥散性调制系统) 由少量核团发出广泛投射,通过 Volume Transmission (容积传输) 在全脑范围调节唤醒、注意、学习、痛觉与情绪等网络属性。
The Secretory Hypothalamus
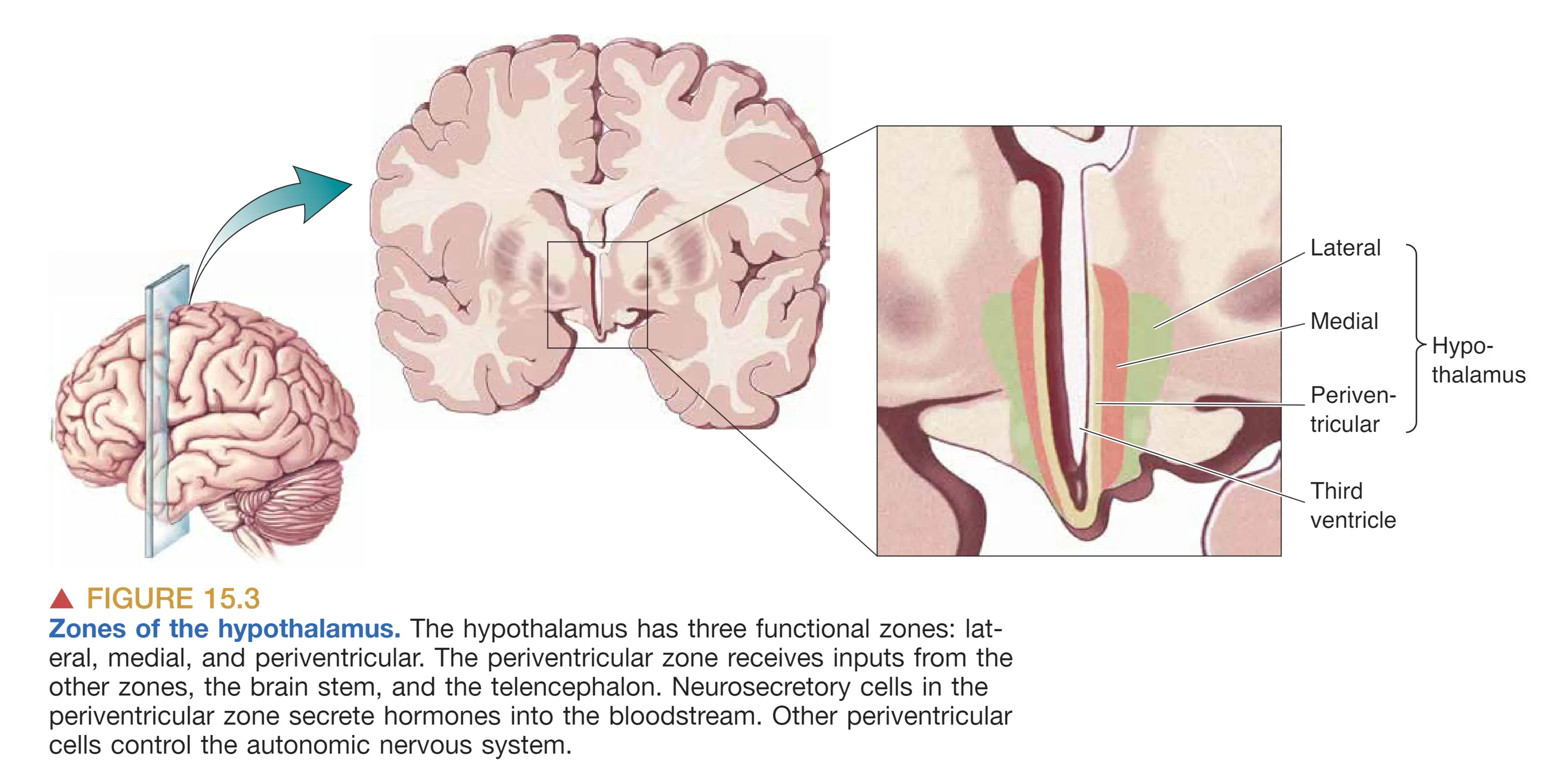
下丘脑(Hypothalamus)构成第三脑室(Third ventricle)的壁,位于背侧丘脑(dorsal thalamus)之下,是维持 Homeostasis (稳态) 的关键中枢:它通过监测体温、血容量与血压、渗透压、能量储备等变量,协调机体对外界变化的适应性反应。每侧下丘脑常被划分为外侧区(lateral zone)、内侧区(medial zone)与 Periventricular Zone (室周区);外侧与内侧区与脑干(brain stem)及端脑(telencephalon)广泛相连,而室周区更突出地承担分泌与整合功能。
室周区中,一群细胞形成 SCN (suprachiasmatic nucleus, 视交叉上核),它将昼夜节律与明暗周期同步(见 [[Chapter19_Sleep]]);同一区域的其他细胞还能调控 ANS 的交感与副交感传出平衡。更关键的是,室周区包含一类 neurosecretory neurons (神经分泌神经元),其轴突向垂体柄(pituitary stalk)延伸,并将激素释放到血液中,从而把神经活动转译为体液信号。
Pathways to the Pituitary
下丘脑通过 Pituitary Gland (垂体) 把神经系统与内分泌系统连接起来。其控制路径分为垂体后叶与垂体前叶两条:后叶是下丘脑组织的直接延伸,采用“轴突运输 → 释放到后叶毛细血管”的方式;前叶是独立的腺体,受下丘脑释放入 Portal Circulation (门脉循环) 的 Hypophysiotropic Hormones (促垂体激素) 调控,进而分泌多种激素影响全身靶腺。
Hypothalamic Control of the Posterior Pituitary
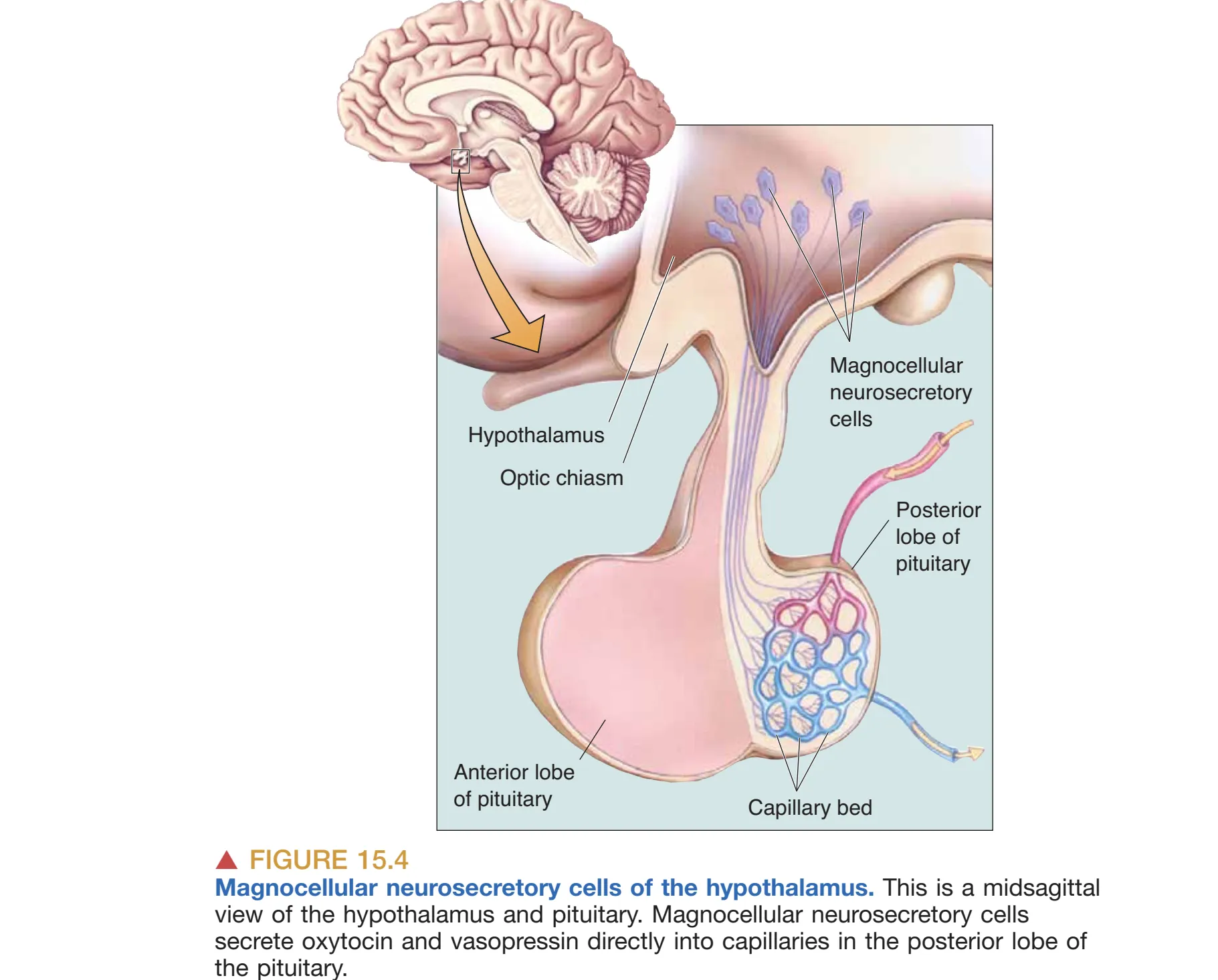
垂体后叶(Posterior Pituitary, 垂体后叶)本质上是下丘脑神经组织的延伸。最大的神经分泌细胞——Magnocellular Neurosecretory Cells (大细胞神经分泌细胞)——将轴突沿垂体柄下行至后叶,并把神经激素(neurohormone)释放入后叶毛细血管。代表性的两种神经激素都是由 9 个氨基酸构成的肽:Oxytocin (催产素/缩宫素) 与 Vasopressin (血管加压素)。催产素在子宫收缩与排乳“射乳反射(letdown reflex)”中不可或缺,同时其在性行为与亲密互动中的上调与社会联结(social bonding)相关,因此常被通俗称为“love hormone”(可见 [[Chapter17_Sex]] 的伴侣依恋讨论)。血管加压素主要作用于肾脏,促进水分保留并减少尿液生成,从而调节血容量与盐浓度;在这一生理语境下它也被称为 Antidiuretic Hormone (ADH, 抗利尿激素)。
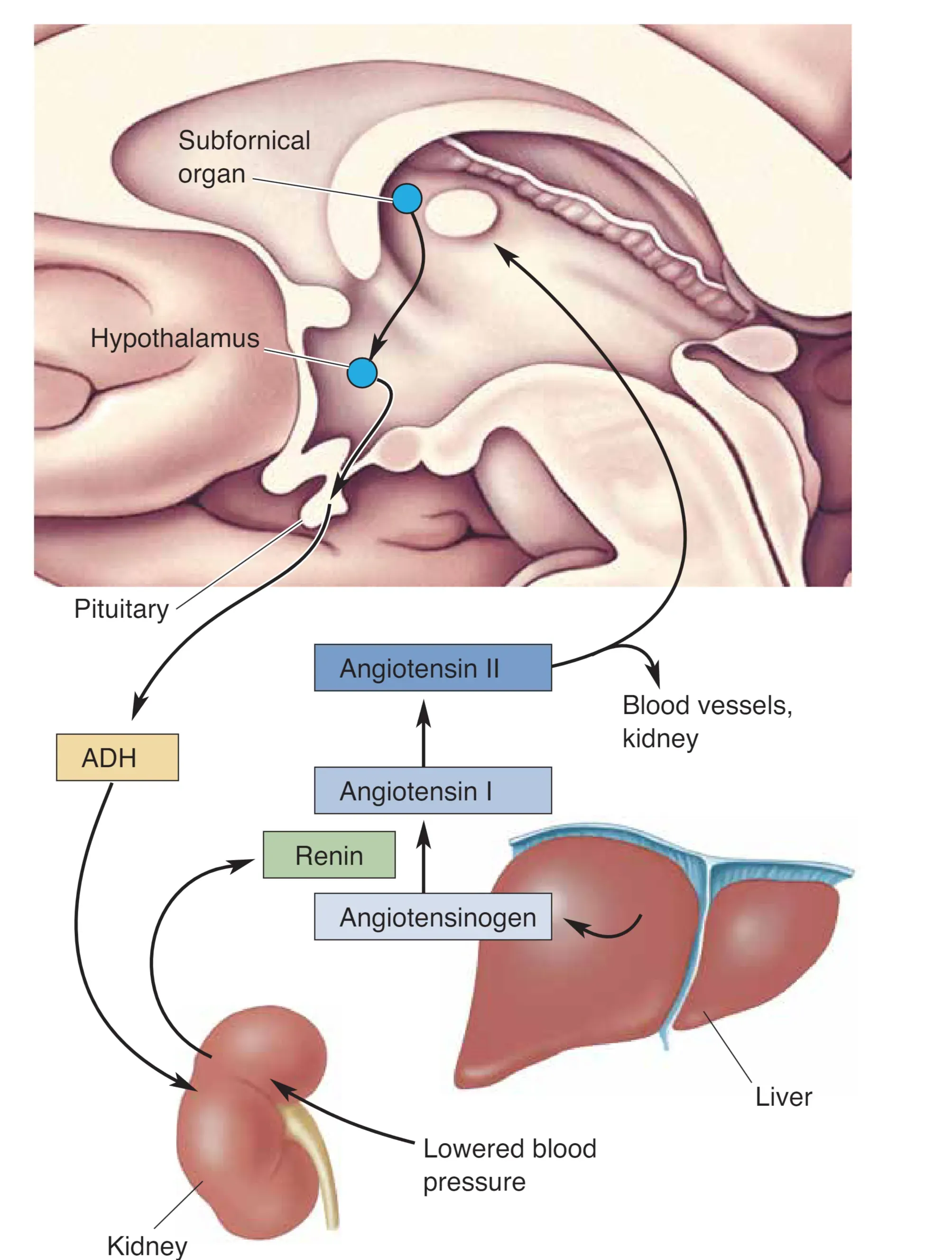
 当血容量与血压下降时,脑与肾的通信呈现出清晰的双向反馈。肾脏将酶 Renin (肾素) 释放入血,使肝脏产生的 Angiotensinogen (血管紧张素原) 先转化为血管紧张素 I,继而裂解为 Angiotensin II (血管紧张素 II)。Angiotensin II 一方面直接作用于肾与血管,另一方面还会被端脑中缺乏血脑屏障的 Subfornical Organ (SFO, 穹窿下器) 感受到;SFO 的神经元随后投射至下丘脑,驱动口渴与相关的体液调节反应(与 [[A_Neurobiology_016_Motivation]] 中的容量性口渴信号可互相印证)。
当血容量与血压下降时,脑与肾的通信呈现出清晰的双向反馈。肾脏将酶 Renin (肾素) 释放入血,使肝脏产生的 Angiotensinogen (血管紧张素原) 先转化为血管紧张素 I,继而裂解为 Angiotensin II (血管紧张素 II)。Angiotensin II 一方面直接作用于肾与血管,另一方面还会被端脑中缺乏血脑屏障的 Subfornical Organ (SFO, 穹窿下器) 感受到;SFO 的神经元随后投射至下丘脑,驱动口渴与相关的体液调节反应(与 [[A_Neurobiology_016_Motivation]] 中的容量性口渴信号可互相印证)。
Hypothalamic Control of the Anterior Pituitary
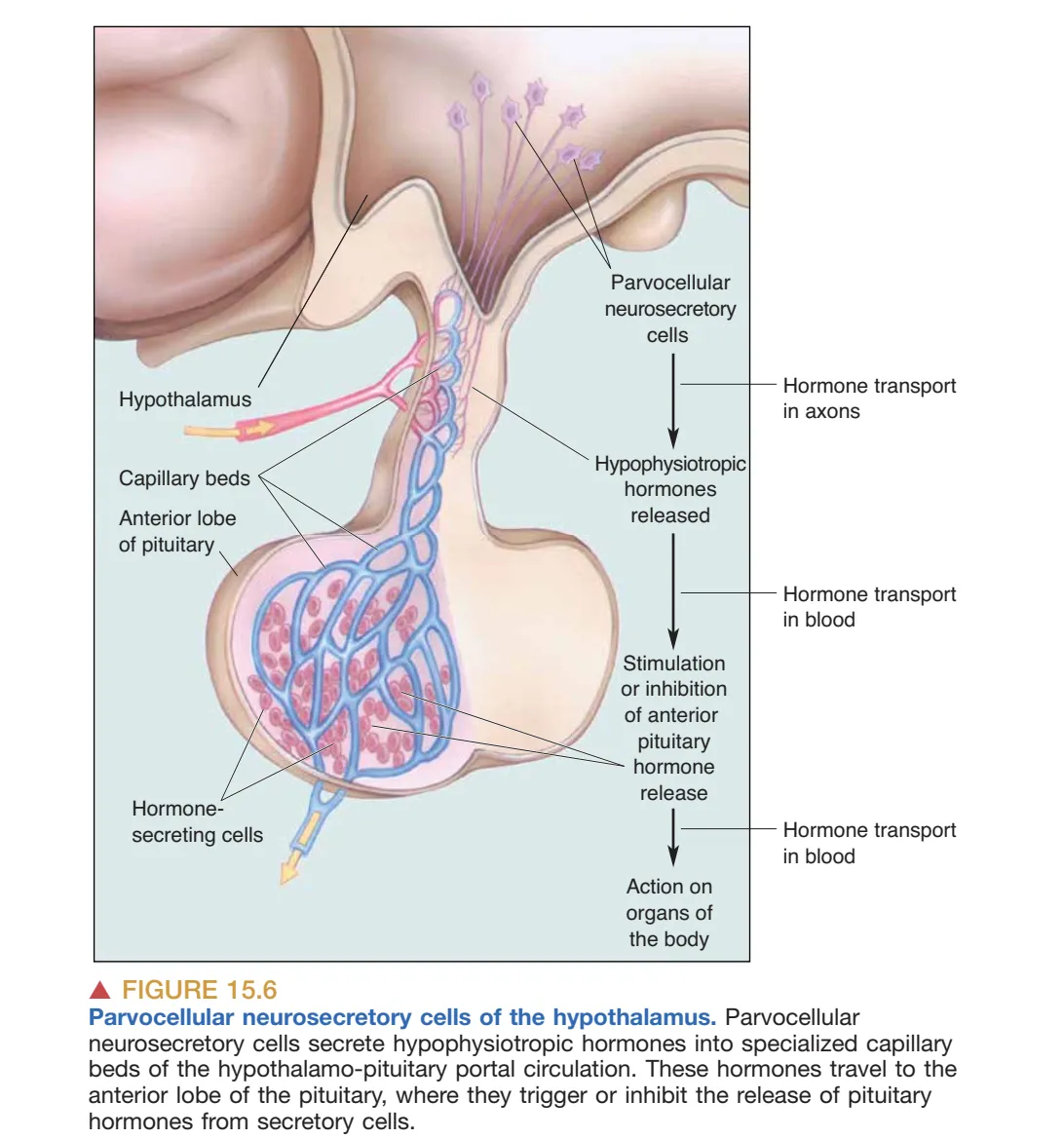
垂体前叶(Anterior Pituitary, 垂体前叶)并非脑组织,而是一个内分泌腺体,能合成并分泌多种激素来调控全身腺体分泌。就层级控制而言,下丘脑才是内分泌系统意义上的“master gland”。这种控制依赖 Parvocellular Neurosecretory Cells (小细胞神经分泌细胞):它们释放的促垂体激素进入下丘脑—垂体门脉系统,随后抵达前叶,刺激或抑制特定垂体激素释放;这些垂体激素进入体循环后再作用于外周靶器官。
 在压力应答中,这一路径构成经典的 HPA Axis (Hypothalamus–Pituitary–Adrenal axis, 下丘脑-垂体-肾上腺轴):室周下丘脑释放 CRH (corticotropin-releasing hormone, 促肾上腺皮质激素释放激素) 至门脉循环,诱发垂体释放 ACTH (adrenocorticotropic hormone, 促肾上腺皮质激素) 入体循环,最终刺激肾上腺皮质释放 Cortisol (皮质醇)。皮质醇属于 Steroid (类固醇激素),与胆固醇相关且脂溶性强,因此相对容易穿过血脑屏障(BBB),既可作用于下丘脑神经元,也可影响其他脑区,从而在能量动员、免疫调节与行为状态上产生广泛影响。
在压力应答中,这一路径构成经典的 HPA Axis (Hypothalamus–Pituitary–Adrenal axis, 下丘脑-垂体-肾上腺轴):室周下丘脑释放 CRH (corticotropin-releasing hormone, 促肾上腺皮质激素释放激素) 至门脉循环,诱发垂体释放 ACTH (adrenocorticotropic hormone, 促肾上腺皮质激素) 入体循环,最终刺激肾上腺皮质释放 Cortisol (皮质醇)。皮质醇属于 Steroid (类固醇激素),与胆固醇相关且脂溶性强,因此相对容易穿过血脑屏障(BBB),既可作用于下丘脑神经元,也可影响其他脑区,从而在能量动员、免疫调节与行为状态上产生广泛影响。
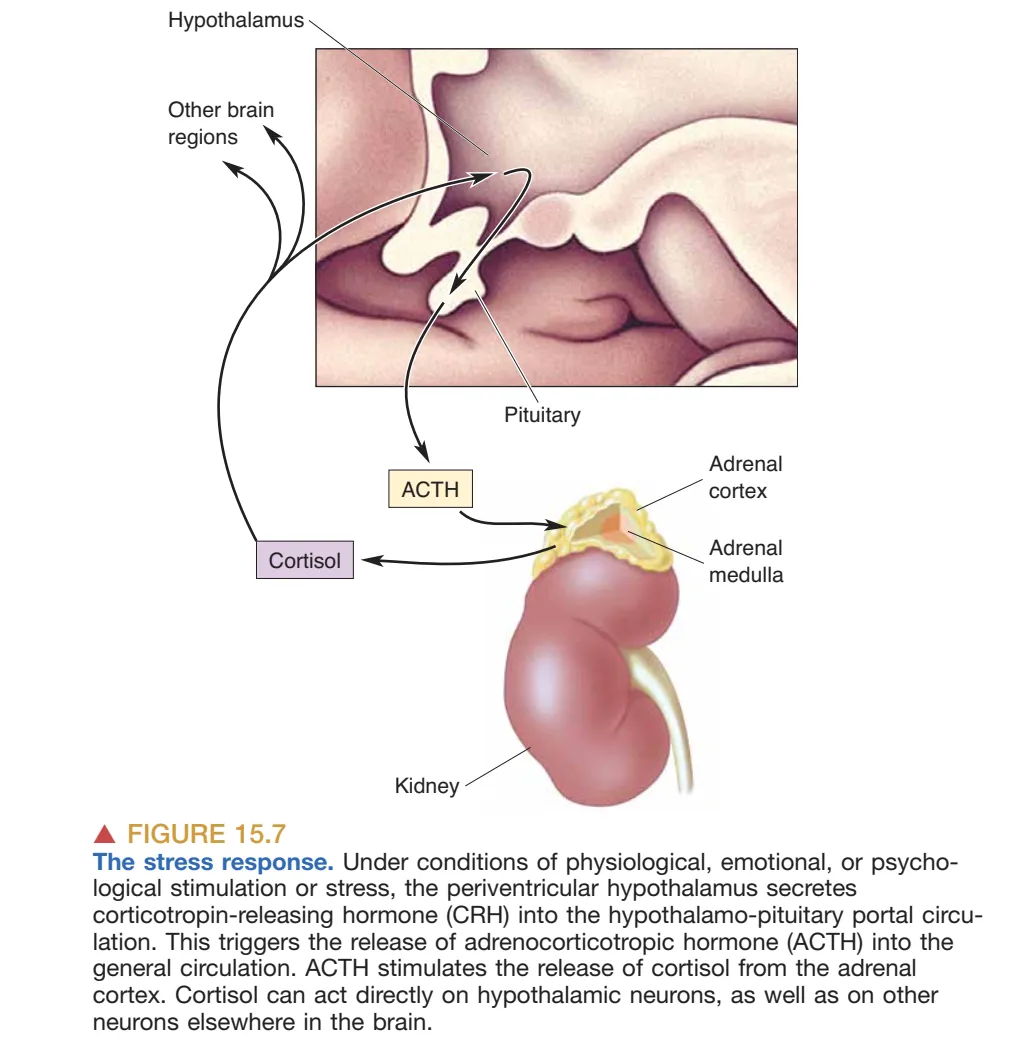 皮质醇的急性升高有适应性意义,但长期高水平皮质醇会损伤海马(Hippocampus)神经元并导致记忆受损,体现为慢性压力对认知的代价,并与 Cushing’s Disease (库欣病/皮质醇过多相关综合征) 的部分症状相关(如体重增加、免疫抑制、失眠以及记忆受损等,且可对全脑功能产生影响)。反向的失衡同样具有临床意义:长期使用强的松 Prednisone(合成皮质醇)可通过负反馈抑制肾上腺功能,导致 adrenal insufficiency(肾上腺功能不全);而 Addison’s disease (艾迪生病) 则代表原发性皮质功能不全所带来的系统性低皮质醇状态。
皮质醇的急性升高有适应性意义,但长期高水平皮质醇会损伤海马(Hippocampus)神经元并导致记忆受损,体现为慢性压力对认知的代价,并与 Cushing’s Disease (库欣病/皮质醇过多相关综合征) 的部分症状相关(如体重增加、免疫抑制、失眠以及记忆受损等,且可对全脑功能产生影响)。反向的失衡同样具有临床意义:长期使用强的松 Prednisone(合成皮质醇)可通过负反馈抑制肾上腺功能,导致 adrenal insufficiency(肾上腺功能不全);而 Addison’s disease (艾迪生病) 则代表原发性皮质功能不全所带来的系统性低皮质醇状态。
The Autonomic Nervous System (ANS)
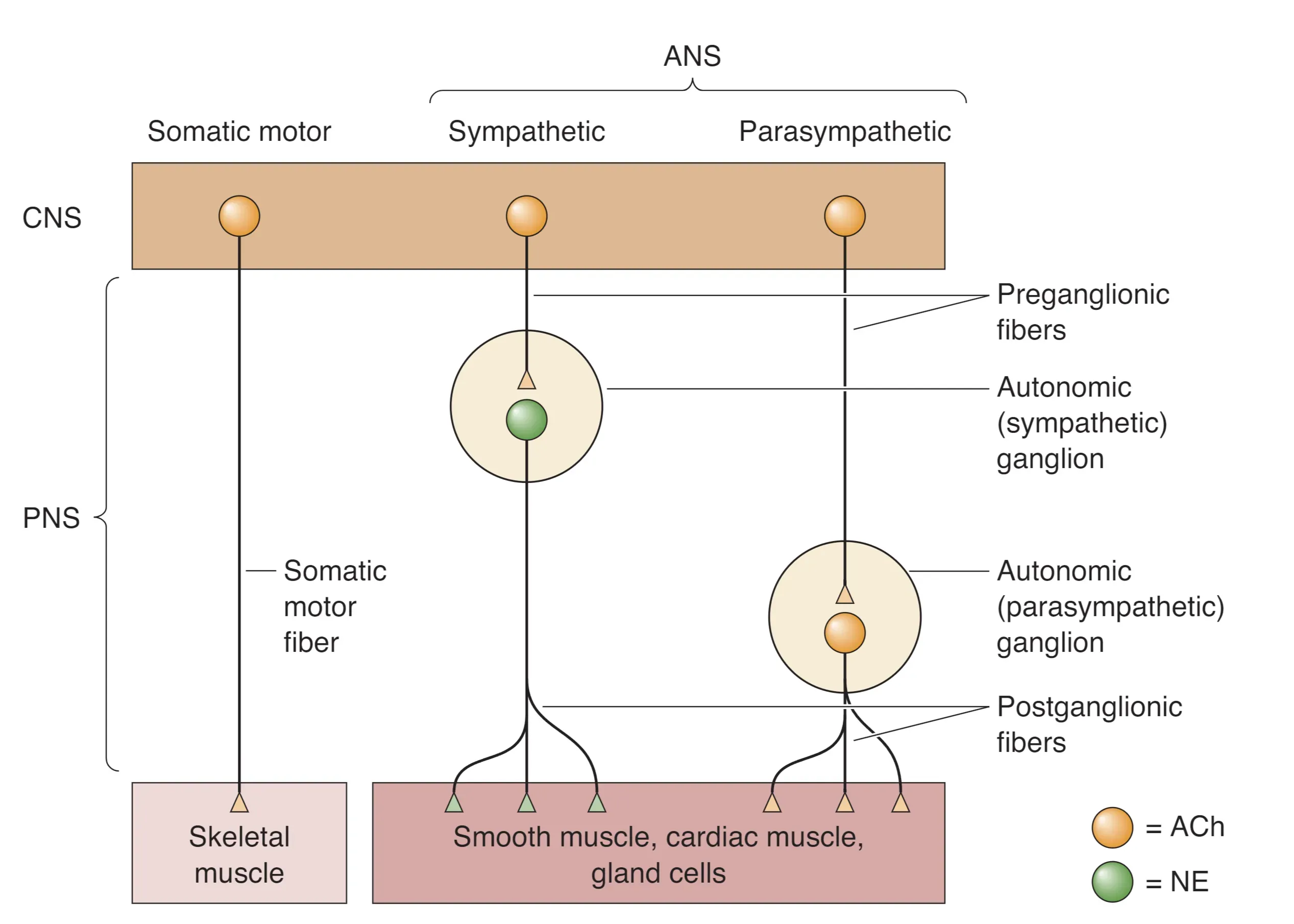
除了调配“激素汤”,室周下丘脑还调控 Autonomic Nervous System (ANS, 自主神经系统),使内脏器官的功能状态与行为情境匹配。ANS 与躯体运动系统共同构成 CNS 的全部输出,但其环路组织更复杂:ANS 的“下运动神经元”细胞体位于 CNS 外的 Autonomic Ganglia (自主神经节),这些节后神经元(postganglionic neurons)受 CNS 内节前神经元(preganglionic neurons;位于脊髓与脑干)驱动,从而形成典型的双神经元通路并支配平滑肌、心肌与腺体。
Functional Divisions
ANS 主要由两条在功能上相对拮抗的分支构成:Sympathetic Division (交感神经) 与 Parasympathetic Division (副交感神经)。交感系统常在“4F”场景中占优——Fight, Flight, Fright, and Sex——其典型效应包括心率与血压上升、消化抑制以及葡萄糖储备动员;副交感系统更偏向“Rest and Digest”,使心率减慢、血压下降、消化功能增强并减少出汗,从而促进能量摄取与储存。
在解剖组织上,交感节前神经元位于脊髓的中间外侧灰质(intermediolateral gray matter),轴突经腹根(ventral roots)离开脊髓并进入椎旁交感链(sympathetic chain)或腹腔等部位的神经节;副交感节前神经元则主要位于脑干核团与脊髓骶段,其对内脏的广泛调控与迷走神经(vagus nerve)密切相关。不同分支在“节后神经元离靶器官的远近”以及“节后递质类型”上也呈现系统性差异。
The Enteric Division
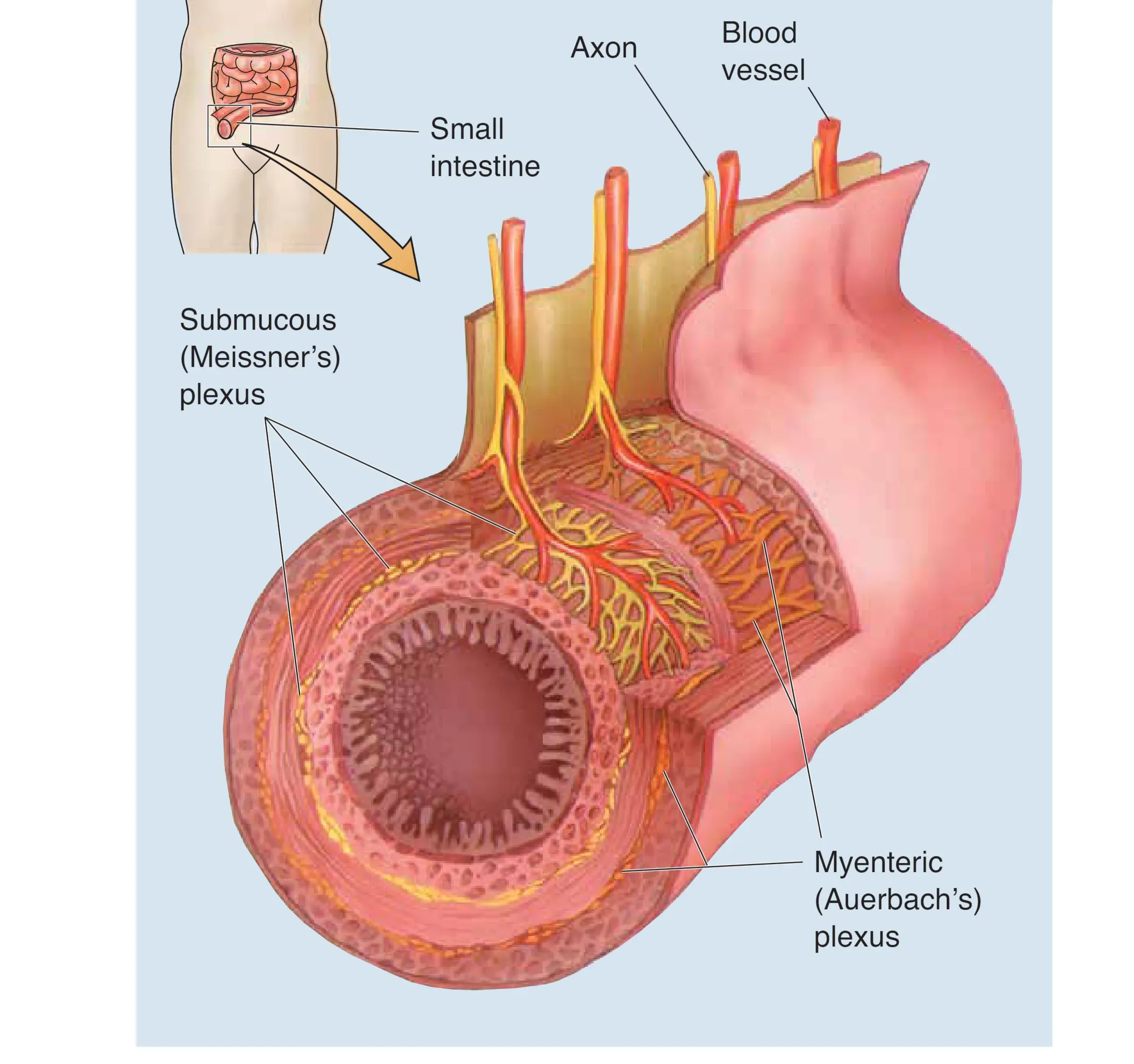
作为 ANS 的第三个重要组成部分,Enteric Division (肠神经部) 被称为“little brain(小脑/第二大脑)”。它嵌入食管、胃、肠道、胰腺与胆囊等消化道壁内,规模并不小,约包含 5 亿个神经元;其由肌间神经丛 Myenteric (Auerbach’s) Plexus (奥尔巴赫神经丛) 与黏膜下神经丛 Submucous (Meissner’s) Plexus (迈斯纳神经丛) 两套复杂网络构成,网络中包含感觉神经、中间神经元与自主运动神经元,能够自主协调从口到肛的食物运输与消化过程。其高度自主性意味着,即便切断与脑的连接,复杂的蠕动反射仍可维持。
+
在中枢层面的调控中,下丘脑被视为自主节前神经元的主要调节者(main regulator of the autonomic preganglionic neuron)。此外,位于延髓并与下丘脑相连的 Nucleus of the Solitary Tract (孤束核) 是内脏信息整合与自主调控的重要中枢之一。
Neurotransmitters and the Pharmacology of Autonomic Function
ANS 外周神经元的主要递质是 Acetylcholine (ACh, 乙酰胆碱):交感与副交感的节前神经元都释放 ACh。ACh 可作用于两类受体——离子型 nAChR (nicotinic ACh receptor, 烟碱型受体) 多与快速 EPSP 相关,而代谢型 mAChR (muscarinic ACh receptor, 毒蕈碱型受体) 通过 GPCR 产生相对缓慢而持久的效应。
在节后环节,副交感节后神经元主要释放 ACh,并几乎完全通过 mAChR 产生局部作用;交感节后神经元在多数部位以 Norepinephrine (NE, 去甲肾上腺素) 为递质,其影响可更弥散,甚至进入血液循环而广泛作用。临床上,Atropine (阿托品) 阻断 mAChR 后会抑制副交感效应,使交感效应相对占优,常表现为心率加快与瞳孔散大。
The Diffuse Modulatory Systems of the Brain
弥散性调制系统(Diffuse Modulatory Systems)是脑内另一类“扩展时空”的化学控制。尽管这些系统使用的递质不同(典型包括 NE、5-HT、DA 与 ACh),它们共享若干结构性原则:每个系统的核心(core)通常只有数千个神经元;多数起源于脑干中心区域;每个神经元的轴突高度分支,单个细胞可影响超过 100,000 个突触后神经元;并且许多突触释放的递质进入细胞外液后可扩散到更大范围,从而形成 Volume Transmission (容积传输)。因此,这些系统更像“全局增益旋钮(gain control)”,改变网络的反应阈值与可塑性,而非直接编码某个具体感觉或运动指令。
Noradrenergic Locus Coeruleus (LC)
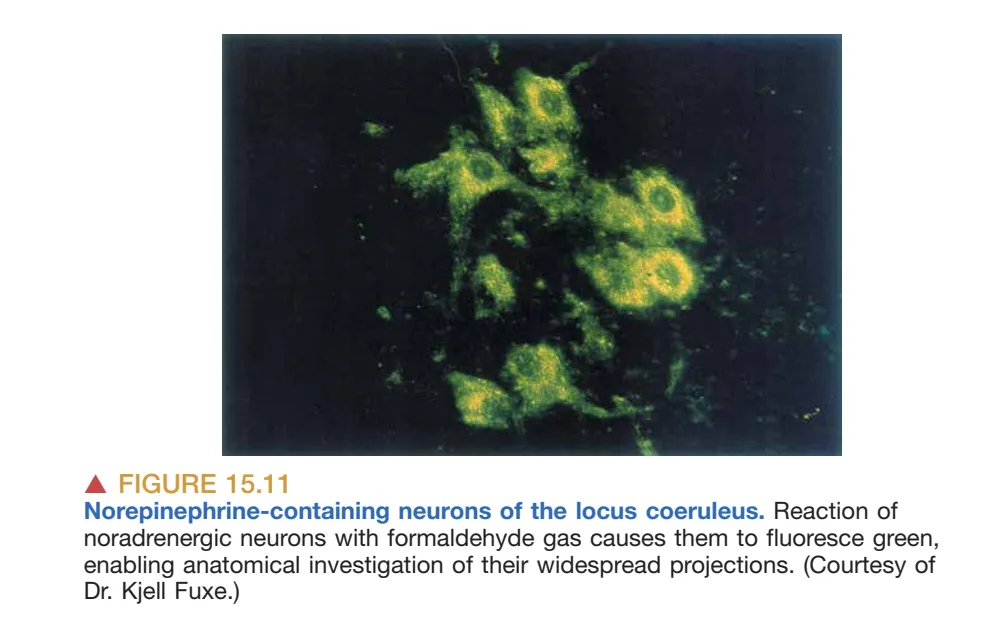
去甲肾上腺素能蓝斑核(Locus Coeruleus, LC)位于脑桥(pons),含有神经黑色素(neuromelanin),左右对称。尽管每侧 LC 约仅 12,000 个神经元,其投射却可覆盖脊髓、小脑、丘脑、下丘脑与新皮层等多个层级,并参与注意(attention)、唤醒(arousal)与睡眠-觉醒节律的调控,同时与学习记忆、焦虑与疼痛、情绪以及脑代谢等过程相关。当个体遭遇新奇或意外刺激时,LC 往往表现出阵发性活跃,从而快速重置警觉状态。
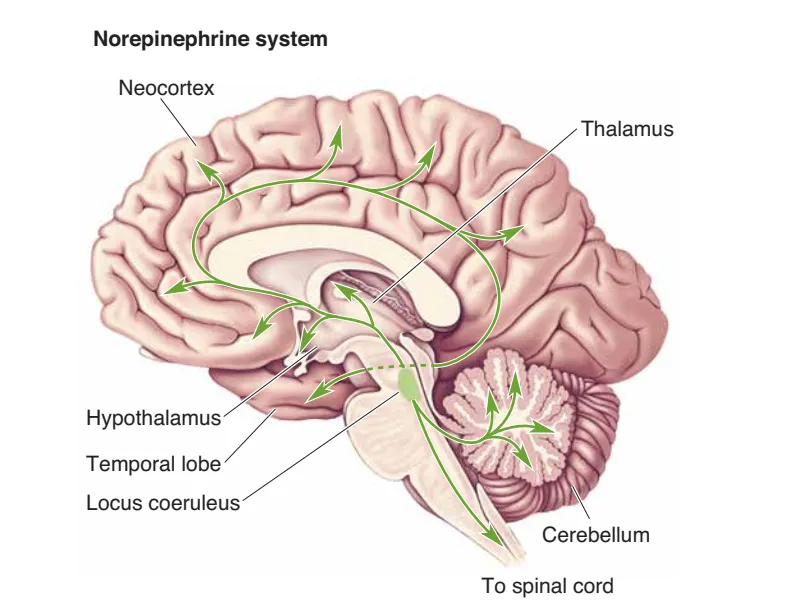
Serotonergic Raphe Nuclei
5-HT(serotonin)神经元主要聚集在 9 个中缝核(Raphe nuclei, 中缝核群)中,沿脑干正中线分布并向 CNS 各层级广泛投射。延髓相关中缝核可向脊髓投射并参与疼痛调制;脑桥与中脑层级的中缝核则以类似 LC 的弥散方式影响大部分脑区。LC 与 raphe 系统常被共同纳入 Ascending Reticular Activating System (ARAS, 上行网状激活系统):该系统在觉醒时放电最快、在睡眠时最低,从而为觉醒状态维持提供化学基础。与代谢状态的联系也可通过饮食与色氨酸(Tryptophan)入脑竞争体现:高碳水饮食往往提升脑内 5-HT 水平,而高蛋白饮食会增加氨基酸竞争,从而降低色氨酸入脑并减少 5-HT 合成潜力。
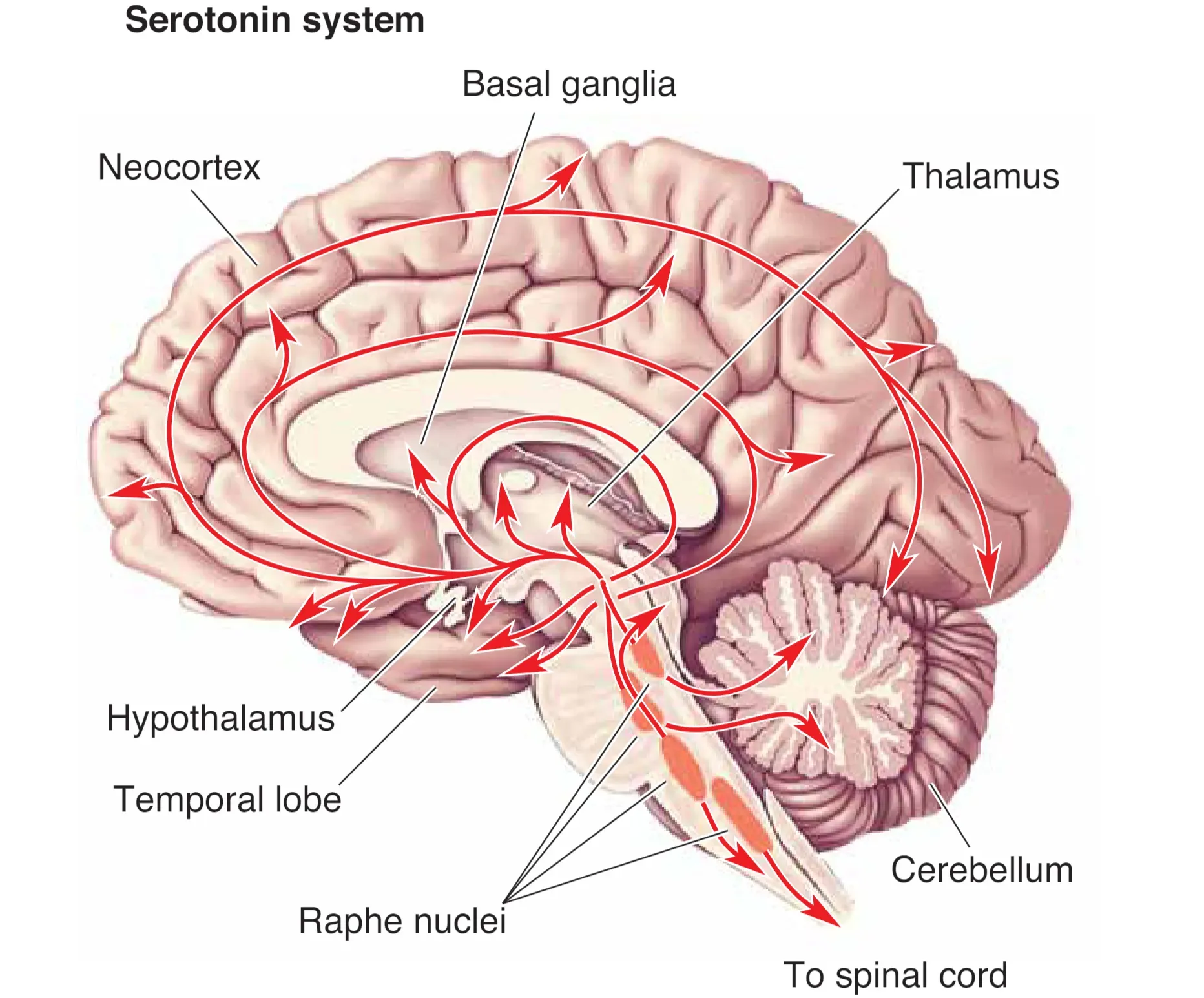
Dopaminergic Substantia Nigra (SN) and Ventral Tegmental Area (VTA)
多巴胺能调制系统的关键起源位于中脑(midbrain)。一条核心通路来自 Substantia Nigra (SN, 黑质) 并投射至纹状体(striatum,包括尾状核与壳核),以尚未完全清楚的机制促进随意运动的启动;该系统退行性变与帕金森病(Parkinson’s disease, PD)密切相关。另一条通路来自 Ventral Tegmental Area (VTA, 腹侧被盖区) 并投射至前额叶与边缘系统在内的端脑区域,常被称为 Mesocorticolimbic Dopamine System (中皮质-边缘多巴胺系统),是奖赏、强化、动机与成瘾的重要神经基础。
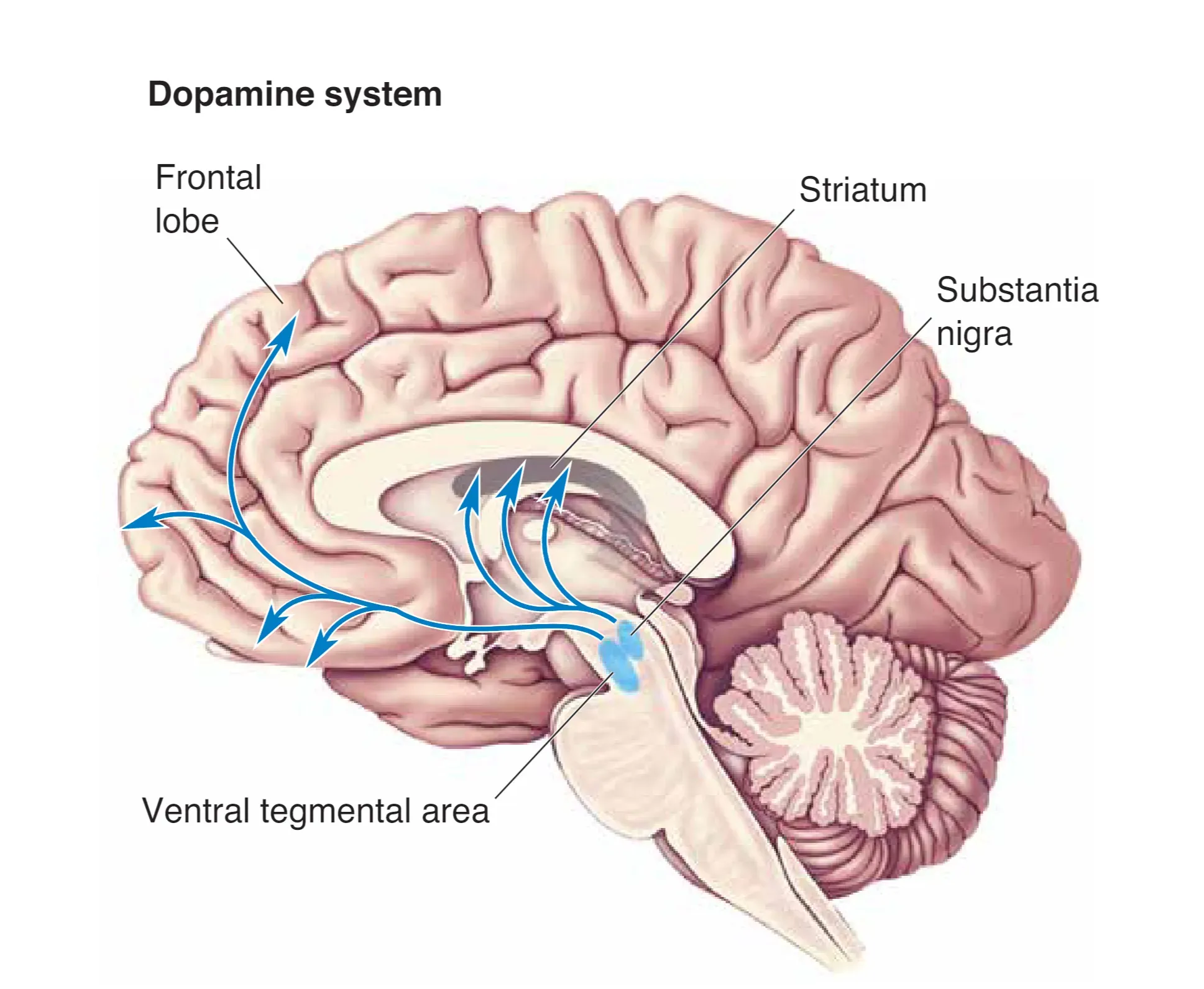
Cholinergic Basal Forebrain and Brain Stem Complexes
胆碱能弥散系统主要包括 Basal Forebrain Complex (基底前脑复合体) 与脑干的 Pontomesencephalotegmental Complex (脑桥-中脑被盖复合体)。基底前脑复合体中的内侧隔核(medial septal nuclei)为海马提供胆碱能支配,而 Meynert 基底核(basal nucleus of Meynert)为新皮层提供主要胆碱能输入;它们与学习、记忆与皮层唤醒密切相关,并在 Alzheimer’s Disease (阿尔茨海默病) 早期出现显著退化。脑桥-中脑被盖复合体主要作用于背侧丘脑(dorsal thalamus),并与去甲肾上腺素与 5-HT 系统协同,调节感觉中继核团的兴奋性。
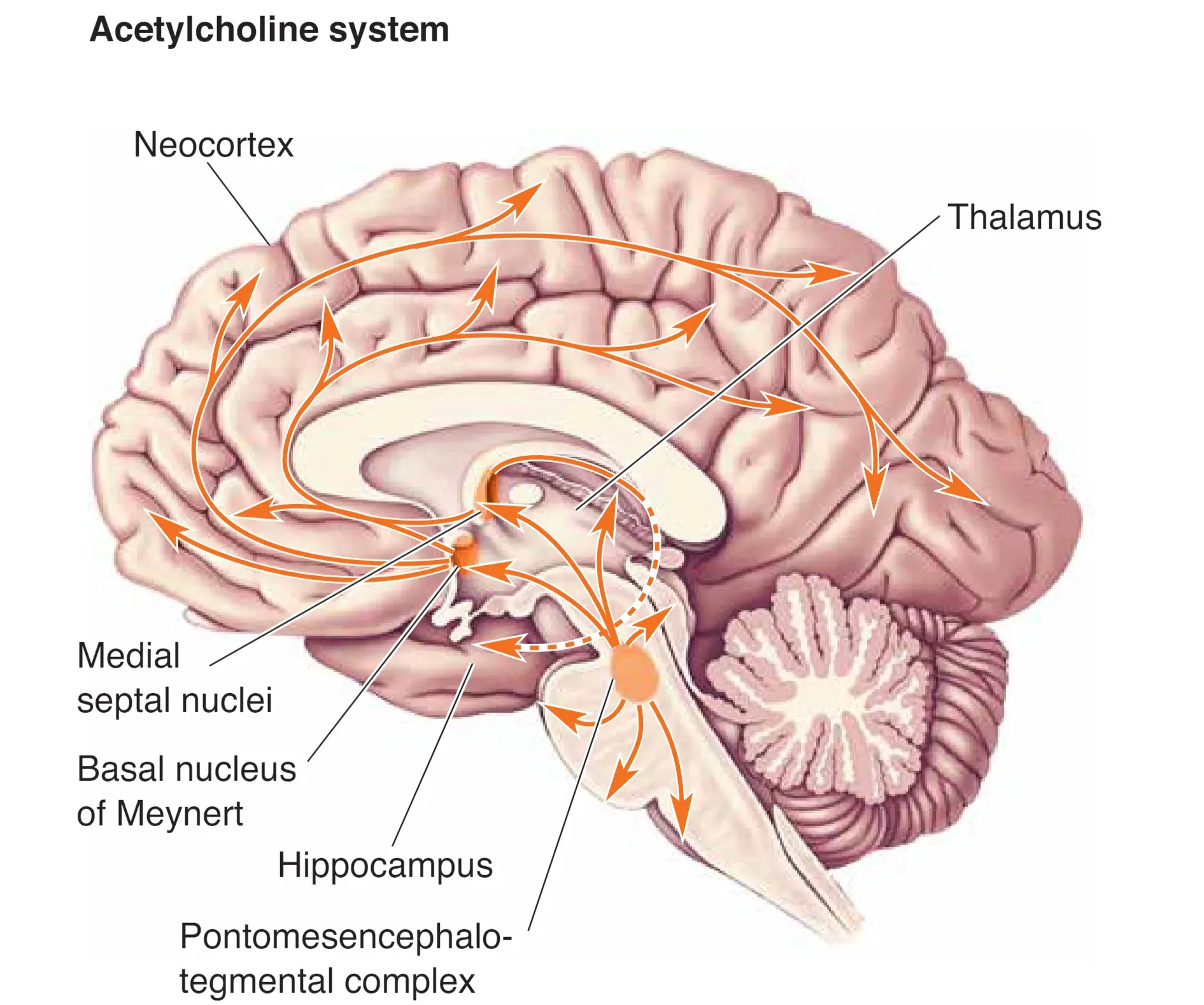
Pharmacology and Drug Action
精神活性药物(Psychoactive drugs)都作用于中枢神经系统,而其中相当一部分效应可以被理解为对弥散性调制系统(尤其是去甲肾上腺素、多巴胺与 5-HT 系统)化学突触传递的干预。
在致幻剂(Hallucinogens)中,Lysergic Acid Diethylamide (LSD, 麦角二乙胺) 的化学结构与 5-HT 相似,被认为是 5-HT 受体的强效激动剂。一个具有解释力的机制强调其对中缝核 5-HT 神经元突触前末梢受体的作用:当 LSD 激活这些受体时,会显著抑制中缝核神经元放电,形成负反馈式抑制;研究者同时也关注 LSD 在大脑皮层的直接作用,这些作用共同导致知觉与现实感的扭曲。
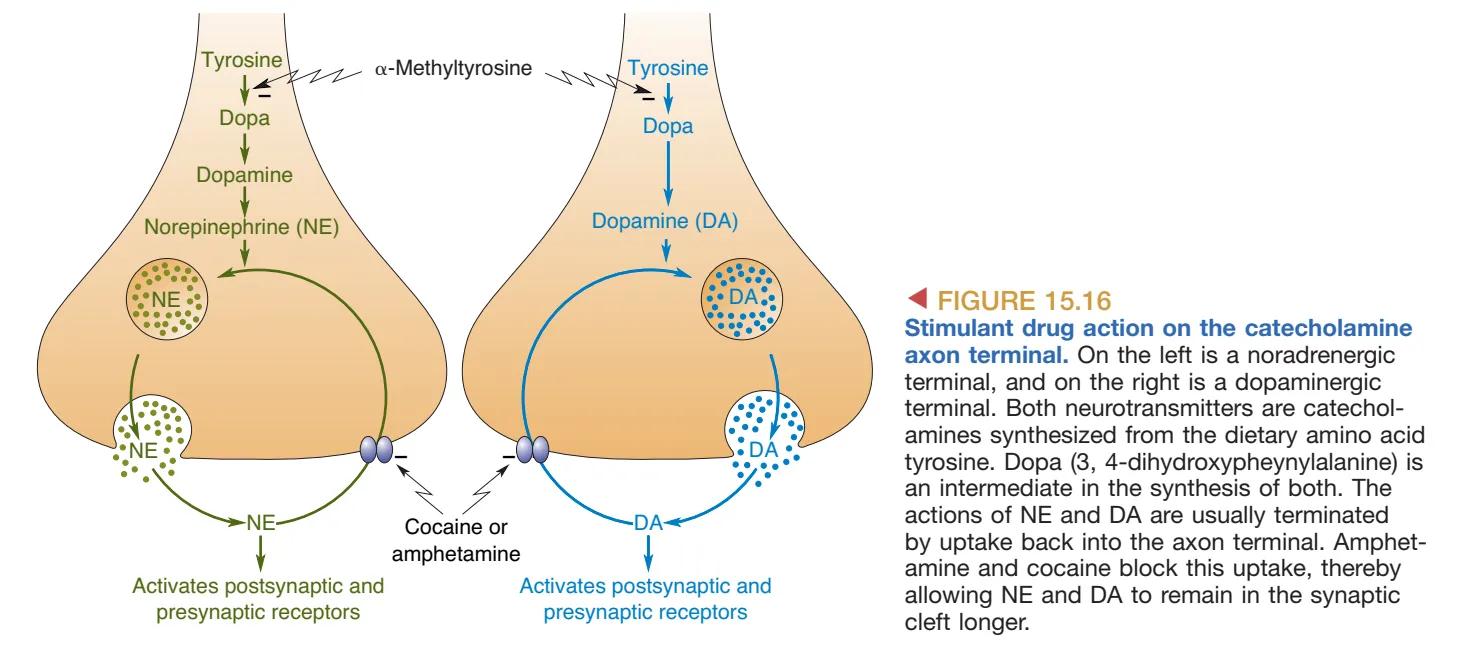
在兴奋剂(Stimulants)中,强力的 Cocaine (可卡因) 与 Amphetamine (安非他命) 都会影响由去甲肾上腺素能与多巴胺能系统形成的突触,阻断 catecholamine uptake (儿茶酚胺再摄取/重摄取),从而增强 NE 与 DA 的突触信号。主观上它们可带来警觉性提高、自信增强以及欣快感(euphoria),但外周层面具有明显的 Sympathomimetic (拟交感) 效应,表现为心率与血压升高、瞳孔散大等;过量摄入可使心血管压力急剧上升并导致心力衰竭,这解释了多起大剂量使用后的意外死亡。
 总之,点对点突触通信更像“精确连线的电报码”,负责快速与局部的信息传递;弥散性调制系统更像“全局增益旋钮”,通过少量核心神经元与容积传输改变大范围网络的反应性;分泌性下丘脑经由血液的内分泌输出则把调控延伸到全身,使行为与内脏状态在同一套化学语言中被统一协调。
总之,点对点突触通信更像“精确连线的电报码”,负责快速与局部的信息传递;弥散性调制系统更像“全局增益旋钮”,通过少量核心神经元与容积传输改变大范围网络的反应性;分泌性下丘脑经由血液的内分泌输出则把调控延伸到全身,使行为与内脏状态在同一套化学语言中被统一协调。
