A_Neurobiology_016_Motivation
Motivation(动机)
动机并不是单一的“想做某事”,而是神经系统把内在需求、稳态偏离、奖赏相关的追逐驱动力与行为输出连接起来的过程:最底层可表现为感觉刺激触发的无意识反射,最高层则可表现为由 frontal lobe(额叶) 神经元启动的有意识运动。
Key ideas
- Homeostasis(稳态) 是动机的基础框架;Hypothalamus(下丘脑) 把体内变量偏离转化为体液、内脏和行为三个层面的协同反应。
- 动机性行为并不只是在“缺什么补什么”;在摄食情境中,长期能量储备与一顿饭内的短期信号共同塑造行为。
- 长期摄食调控围绕 leptin(瘦素) 与下丘脑弓状核—室旁核—下丘脑外侧区回路展开;短期摄食调控则整合 ghrelin、胃扩张、CCK、insulin 等信号。
- mesocorticolimbic dopamine system(中脑-皮层-边缘多巴胺系统) 与强化、奖赏相关的追逐驱动力和行为固化有关,说明动机还包含“wanting(渴望)”这一成分。
- 饮水与体温调节提示:动机并不限于摄食,它也是下丘脑组织生存行为的一般方式。
Abstract / 研究概要
动机(Motivation)可理解为机体为了满足内在需求而启动行为的过程。可将其置于稳态(Homeostasis)框架下讨论:当血容量、渗透压、能量储备或体温等变量偏离适宜范围时,下丘脑通过体液反应、内脏运动反应与躯体运动反应组织纠偏。摄食是这一框架中最典型的例子,其中长期调控围绕体脂储备与 leptin 信号展开,短期调控则围绕一顿饭内的饥饿信号与饱腹信号展开。与此同时,奖赏与强化回路说明,动机并不完全等同于稳态恢复:多巴胺系统更多关联奖赏相关的追逐驱动力,而 5-HT 系统则为食物与情绪之间的联系提供背景。除摄食外,饮水与体温调节也展示了下丘脑如何把生理偏差转译为行动。
1. 从“需要”到“行动”:动机的层级与基本定义
行为发起可以放在一个从低到高的层级上理解:最低层级是由感觉刺激引发的无意识反射,最高层级则是由 frontal lobe(额叶) 神经元启动的有意识动作。在这一连续体中,voluntary movements(自愿运动) 之所以发生,是因为机体需要被满足;换言之,动机不是附加在行为之外的标签,而是让行为得以被“发动”的条件。
如果从功能角度概括,动机性行为(motivated behavior)就是把内部需求转化为外部反应的神经过程。这个过程与下丘脑紧密联系:当机体偏离稳态时,下丘脑并不只“检测异常”,而是把异常组织成一套有方向的输出,使行为朝纠正偏差的方向推进。因此,动机既包含需求的产生,也包含对合适反应方式的选择。
[!note] 对本章而言,最重要的出发点不是“人为什么会想要某物”,而是“当身体状态失衡时,神经系统如何把这种失衡转化为一套可执行的反应”。
2. 下丘脑、稳态与动机性行为
Hypothalamus(下丘脑) 是动机与稳态调节的枢纽。其基本逻辑是:下丘脑接收与体内状态有关的感觉转导信息,然后组织一套通常由三部分构成的反应。第一部分是 Humoral response(体液反应),即刺激或抑制垂体激素释放;第二部分是 Visceromotor response(内脏运动反应),即调整自主神经系统(ANS)的交感/副交感平衡;第三部分是 Somatic motor response(躯体运动反应),即驱动机体采取合适的行为。
在这一框架下,动机性行为并不是与内分泌和自主神经反应分离的“高层心理现象”,而是三类输出中的行为性部分。许多纠正稳态偏离的行为与 lateral hypothalamic area, LHA(下丘脑外侧区) 有关;更概括地说,室周区和内侧区更偏向体液与内脏反应,而行为动作的最终发起更依赖外侧区。这一组织方式也解释了为什么同样是下丘脑损伤,不同区域会导致截然不同的摄食、饮水或体温反应。
3. 摄食行为的长期调控:体脂储备如何塑造动机
3.1 Lipostatic hypothesis 与 leptin 信号
关于长期摄食调控,可以围绕 Lipostatic hypothesis(恒脂假说) 展开:大脑监测脂肪储备,并试图把体重或体脂维持在某个设定值附近。与这一假说相配套的关键信号是 leptin(瘦素)。Leptin 由脂肪细胞释放进入血液,并作用于下丘脑 arcuate nucleus(弓状核) 上的 leptin 受体神经元,因此它可以被看作体脂水平进入脑内调控回路的入口信号。
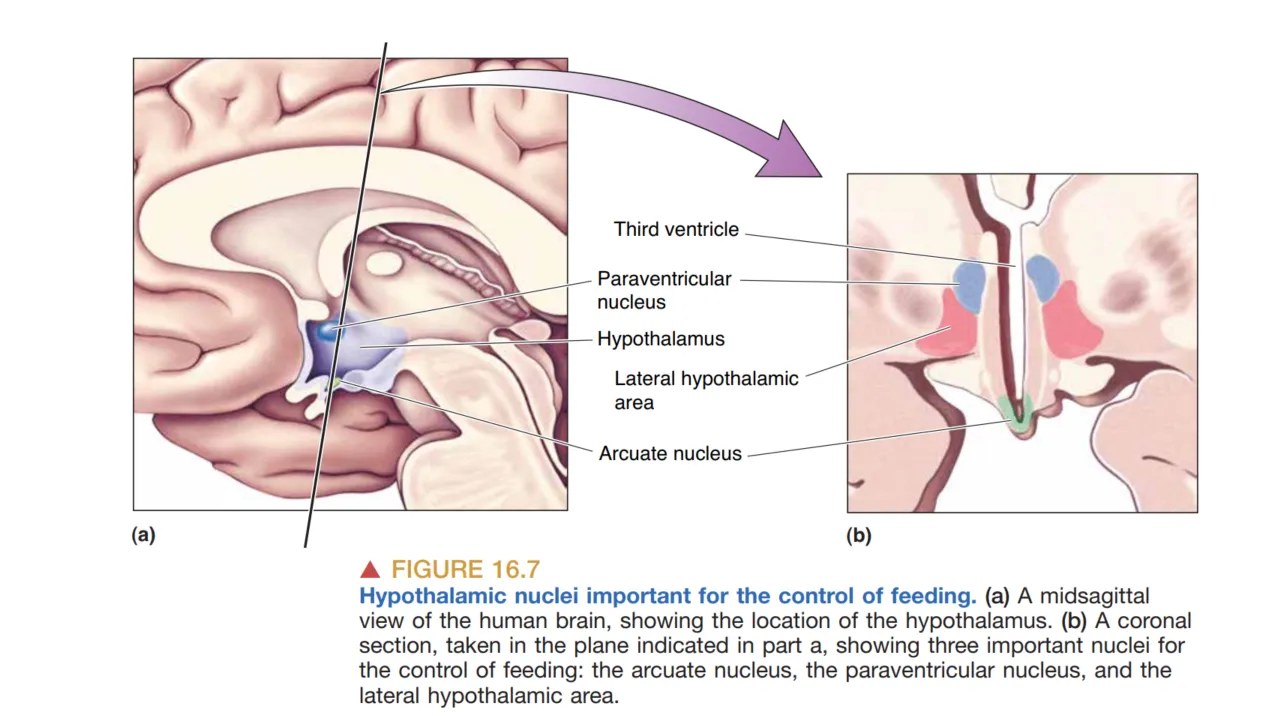 弓状核中至少包含两类对摄食具有相反作用的肽能神经元。其一是释放 MSH 与 CART 的神经元;当 leptin 水平升高时,这组神经元更活跃,形成与“少吃、代谢增加”一致的反应模式。其二是释放 NPY 与 AgRP 的神经元;当 leptin 水平下降时,它们被激活,形成与“多吃、代谢降低”一致的反应模式。因此,长期摄食调控并不是一个单向的抑制系统,而是两套相反的肽能信号在下丘脑回路中动态平衡的结果。
弓状核中至少包含两类对摄食具有相反作用的肽能神经元。其一是释放 MSH 与 CART 的神经元;当 leptin 水平升高时,这组神经元更活跃,形成与“少吃、代谢增加”一致的反应模式。其二是释放 NPY 与 AgRP 的神经元;当 leptin 水平下降时,它们被激活,形成与“多吃、代谢降低”一致的反应模式。因此,长期摄食调控并不是一个单向的抑制系统,而是两套相反的肽能信号在下丘脑回路中动态平衡的结果。
3.2 Leptin 升高:anorectic peptides 的模式
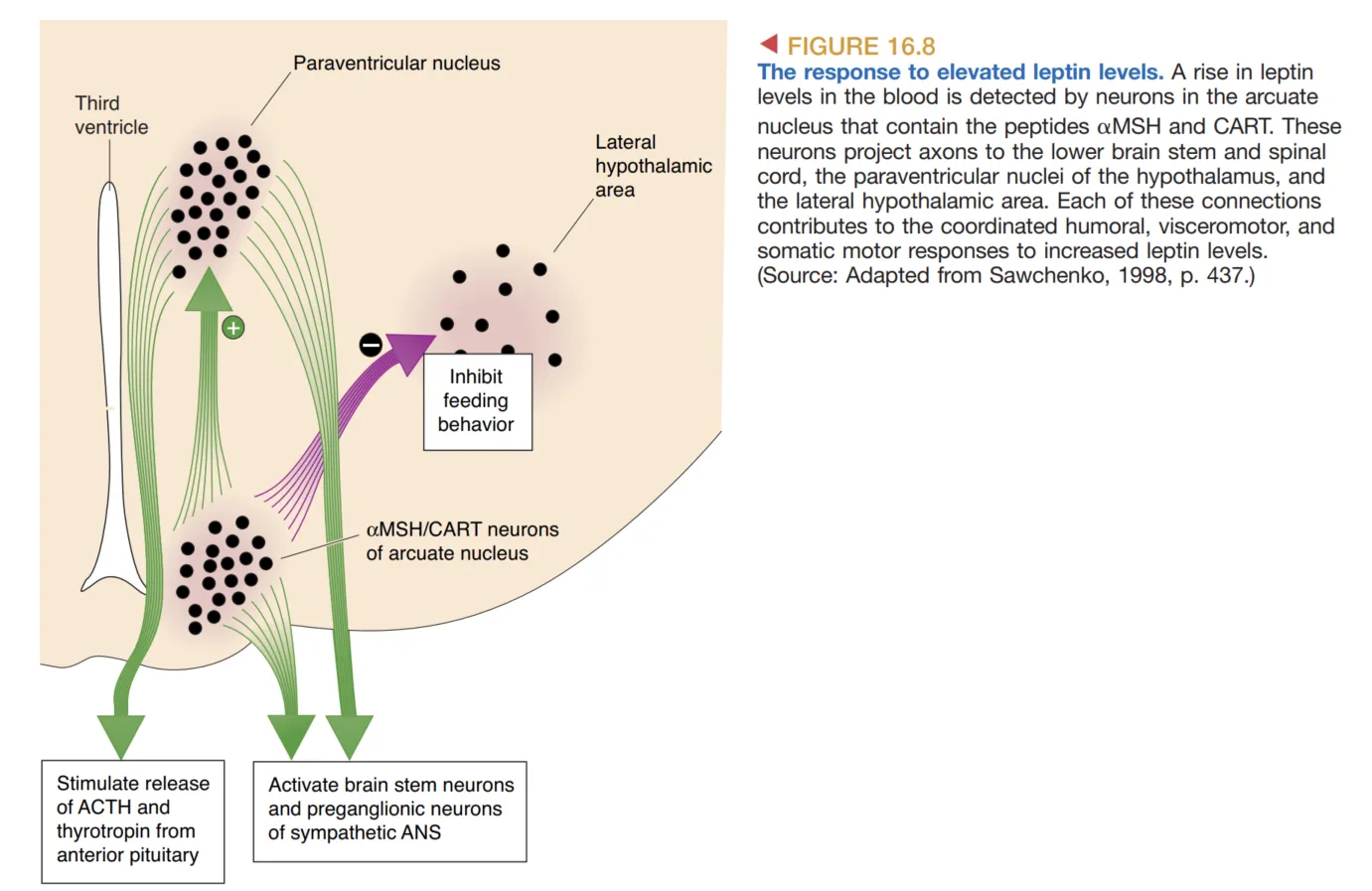 当 leptin 水平升高时,弓状核的 MSH/CART 神经元驱动一套典型的 anorectic peptides(厌食肽) 反应。这一反应可拆成三个层面:体液层面上,室旁核相关通路促进 TSH 与 ACTH 分泌;内脏层面上,交感神经张力增强;行为层面上,摄食行为下降。换句话说,高 leptin 状态不仅表示“体脂较多”,还意味着机体正在向“减少摄入、提高消耗”的方向调整。
当 leptin 水平升高时,弓状核的 MSH/CART 神经元驱动一套典型的 anorectic peptides(厌食肽) 反应。这一反应可拆成三个层面:体液层面上,室旁核相关通路促进 TSH 与 ACTH 分泌;内脏层面上,交感神经张力增强;行为层面上,摄食行为下降。换句话说,高 leptin 状态不仅表示“体脂较多”,还意味着机体正在向“减少摄入、提高消耗”的方向调整。
这些信号部分通过 paraventricular nucleus, PVN(室旁核) 与 lateral hypothalamic area(下丘脑外侧区) 实现。就功能上说,PVN 更接近把代谢状态转化为内分泌输出,而 LHA 更接近把这些状态转化为进食行为是否被启动。因此,leptin 对摄食的抑制并不是单一核团的作用,而是多核团协调的结果。
3.3 Leptin 降低:orexigenic peptides 的模式
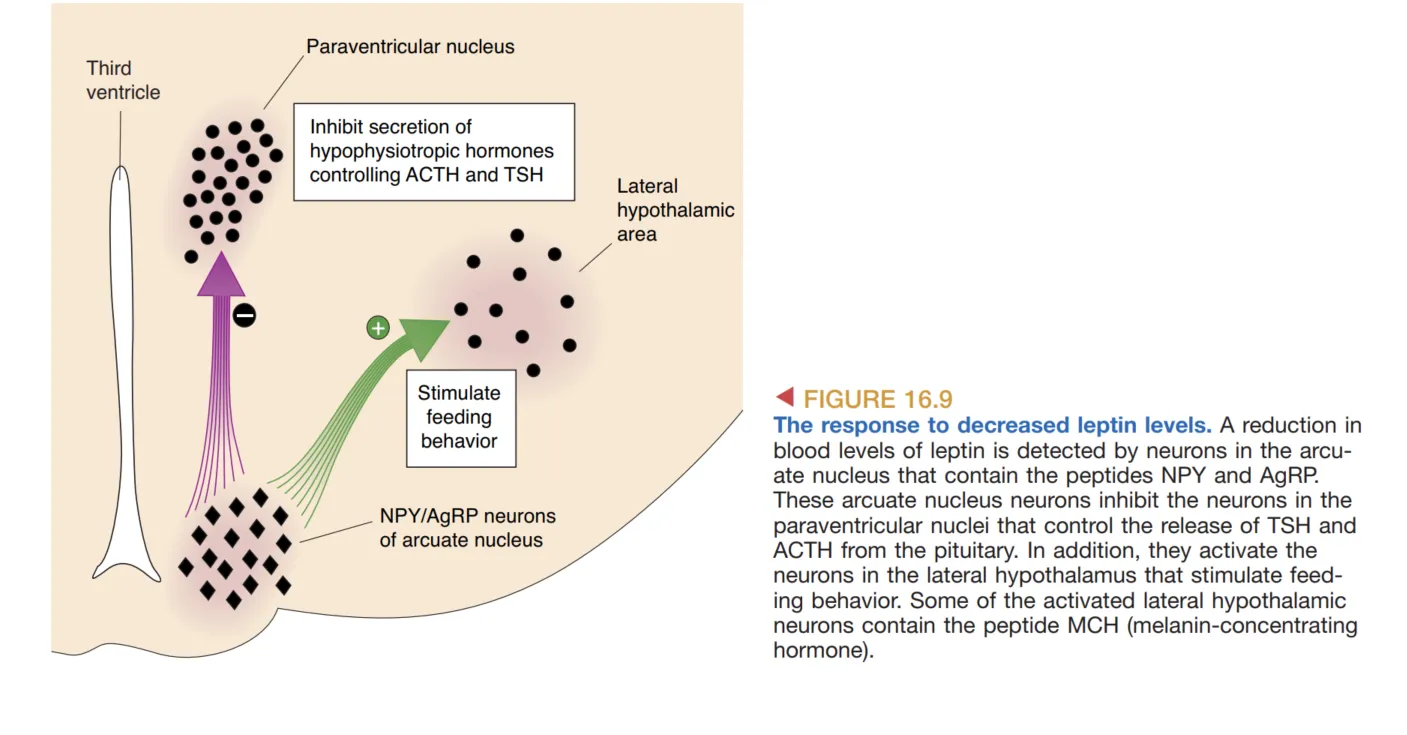 当 leptin 水平降低时,前述抑制模式被关停,同时另一类弓状核神经元被激活,即释放 NPY(neuropeptide Y) 与 AgRP(agouti-related peptide) 的神经元。这一组信号可概括为 orexigenic peptides(促食欲肽)。这一组信号会抑制室旁核中与 TSH/ACTH 释放相关的神经元、增强副交感神经活动,并激活下丘脑外侧区中促进摄食的神经元,最终表现为摄食增加、代谢下降。
当 leptin 水平降低时,前述抑制模式被关停,同时另一类弓状核神经元被激活,即释放 NPY(neuropeptide Y) 与 AgRP(agouti-related peptide) 的神经元。这一组信号可概括为 orexigenic peptides(促食欲肽)。这一组信号会抑制室旁核中与 TSH/ACTH 释放相关的神经元、增强副交感神经活动,并激活下丘脑外侧区中促进摄食的神经元,最终表现为摄食增加、代谢下降。
这里的关键点不是某一种递质“单独导致饥饿”,而是低 leptin 状态重新配置了整个下丘脑网络,使内分泌、自主神经与行为三类输出同时朝能量获取方向偏移。因此,长期摄食调控本质上是一种全身资源管理,而不是孤立的“胃口变化”。
3.4 LHA 肽类、MC4 receptor 与损伤线索
LHA(下丘脑外侧区) 可被视为长期摄食调控的行为输出端。其中特别重要的两类肽是 MCH(melanin-concentrating hormone,黑色素聚集激素) 与 orexin(食素/促食欲素,也称 hypocretin)。前者与延长进食有关,倾向于促进睡眠,后者促进进食启动,并与觉醒相关。在 leptin 降低时,这两类肽信号都会增加;其中部分 MCH 神经元与大脑皮层存在广泛连接,因此该系统可能把能量状态变化传递到更大范围的脑网络,但具体机制在本章材料中未进一步展开。
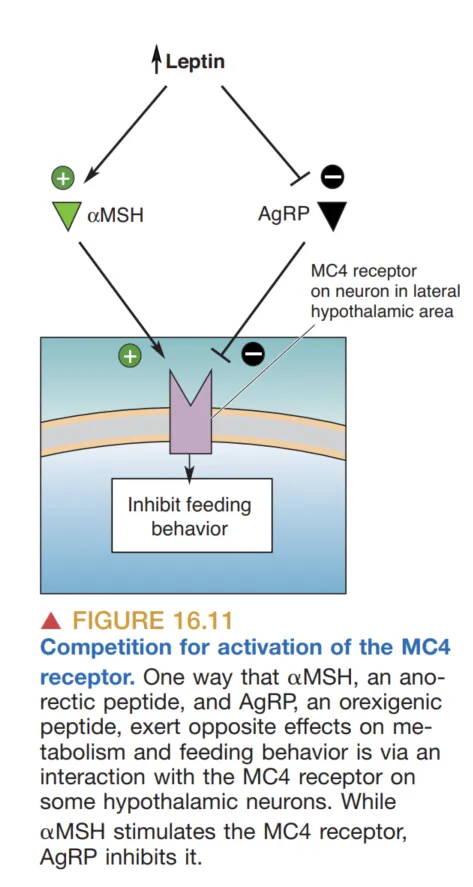
在受体层面,AgRP 与 MSH 被记录为在 MC4 receptor(MC4 受体) 上呈拮抗关系,这为“促进进食”与“抑制进食”的竞争关系提供了分子层面的简化表述。病理与损伤线索也支持这一框架:双侧下丘脑小损伤即可显著改变后续摄食与脂肪储备;双侧 lateral hypothalamus 损伤可导致摄食显著减少(lateral hypothalamic syndrome),而双侧 ventromedial hypothalamus 损伤则与过度进食和肥胖相关。
3.5 能量平衡情境
长期摄食调控还依赖基本的能量平衡背景。这里可区分 prandial state(膳食状态) 与 postabsorptive state(吸收后状态):前者指血液中充满营养物质的状态,后者指两餐之间不进食的状态。这个区分的意义在于,它提醒我们:同一种食欲信号并不是在真空中起作用,而是在“刚进食完”与“长期未进食”的不同代谢背景下被解释。
4. 摄食行为的短期调控:一顿饭如何被启动与终止
4.1 三个阶段
一次进食过程可拆为三个连续阶段:Cephalic phase(头期)、Gastric phase(胃期) 与 Substrate phase(底物期/肠期)。头期由食物的视觉、嗅觉、味觉甚至“想到食物”触发,并伴随唾液与消化液分泌;此时副交感与 enteric division(肠神经部) 的活动已经开始为进食做准备。胃期对应咀嚼、吞咽以及胃内容物增加时的反应,而底物期则对应营养物质开始进入血液后的状态变化。
这个分期强调:短期摄食调控并不是“吃到饱才出现反馈”,而是在进食前、进食中、吸收后都存在信号更新。也因此,一顿饭的起点和终点都不是单一分子决定,而是多类信号逐步接力的结果。
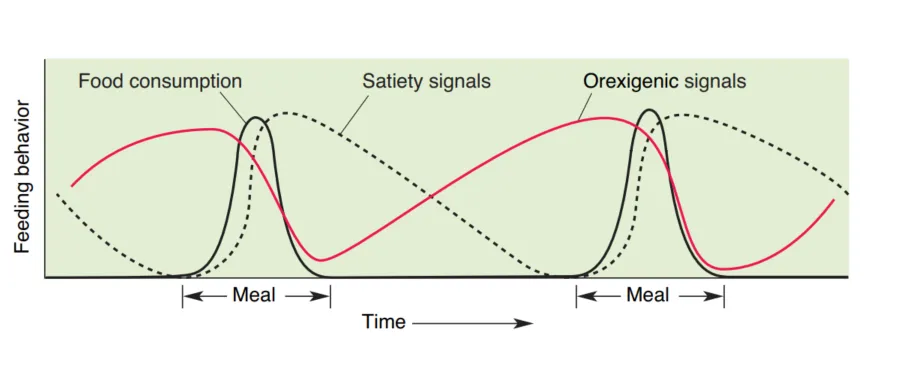
4.2 Orexigenic signal:ghrelin
短期促食欲信号中,最典型的是 Ghrelin(促生长激素释放素)。空腹时胃释放 ghrelin;其升高可激活弓状核中含 NPY/AgRP 的神经元,因此与“饭前启动摄食”的状态相联系。材料甚至以拟声方式强调 ghrelin 与“肚子咕咕叫”的直观关联,说明它可被视为短期饥饿的代表性信号。
4.3 Satiety signals:胃扩张、CCK 与 insulin
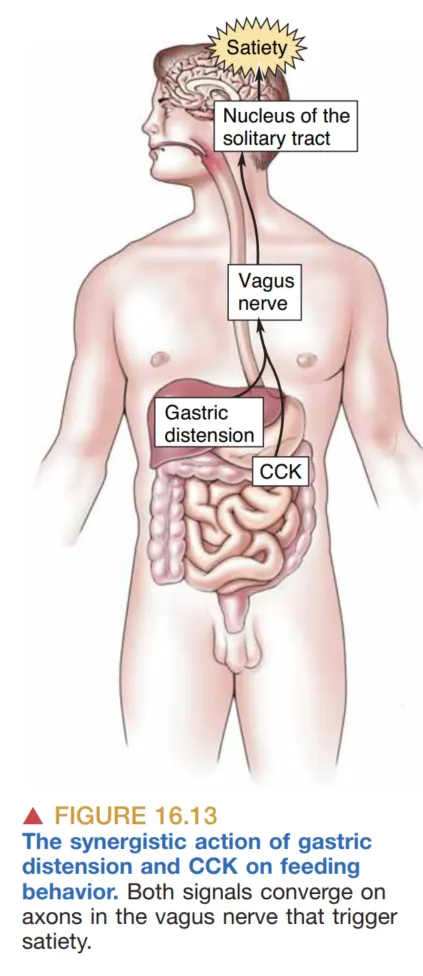
与 ghrelin 相对,短期饱腹信号来自多层次反馈。其一是 Gastric distension(胃扩张):胃壁拉伸会激活机械感受性轴突,多数通过 vagus nerve(迷走神经) 上行至延髓的 nucleus of the solitary tract / solitary tract nucleus(孤束核),从而抑制摄食行为。其二是 CCK(cholecystokinin,胆囊收缩素):CCK 来自肠道上皮细胞与部分 enteric nervous system 神经元,尤其在脂肪刺激下释放,并主要通过迷走神经感觉轴发挥饱腹作用,减少进食频率与进食量。
其三是 Insulin(胰岛素)。Insulin 由胰腺 细胞释放,也是重要的代谢激素;它可直接作用于下丘脑弓状核和腹内侧核以抑制摄食。另有课堂补充指出,insulin 在头期、胃期和底物期都可出现阶段性上升,并在底物期达到最高峰。这提示 insulin 既属于代谢激素,也参与对一顿饭内摄食行为的动态调节。
4.4 其他短期因素
Marijuana 可通过 CB1 受体 增加食欲。这一条虽然在整章中所占篇幅不大,但它提醒我们:短期摄食调控并不只受经典内脏信号控制,奖赏与药理因素同样可以改变进食阈值。
5. 为什么我们会吃:奖赏、强化与情绪
5.1 Reinforcement and Reward
在“Why do we eat?”这个问题上,摄食可以从单纯能量补给扩展到奖赏与强化层面。electrical self-stimulation(自我刺激) 现象提示,只要某些脑区被激活,动物就会重复执行导致该刺激出现的行为;因此,奖赏并不只是体验上的“好”,它还能强化(reinforce)一个行为习惯,使其更容易再次发生。
5.2 Dopamine 与 wanting
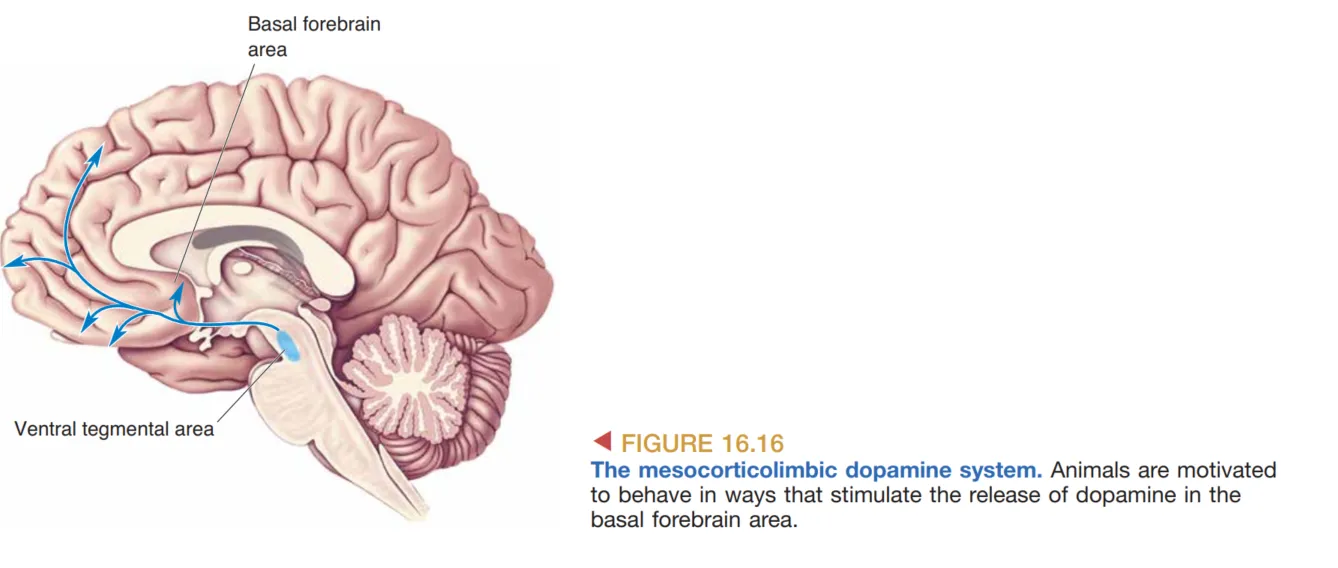 与这种强化最相关的通路是 mesocorticolimbic dopamine system(中脑-皮层-边缘多巴胺系统),起源于 VTA(腹侧被盖区)。这条通路与动机、奖赏和成瘾联系在一起,同时也需要区分 Liking(愉悦感) 与 Wanting(渴望):在这一整理框架中,多巴胺更接近“想要、追求奖赏”的行为驱动力,而不完全等于奖赏本身的快感体验。因此,动机并不只涉及是否获得愉悦,也涉及机体是否会持续朝某个目标投入行为。
与这种强化最相关的通路是 mesocorticolimbic dopamine system(中脑-皮层-边缘多巴胺系统),起源于 VTA(腹侧被盖区)。这条通路与动机、奖赏和成瘾联系在一起,同时也需要区分 Liking(愉悦感) 与 Wanting(渴望):在这一整理框架中,多巴胺更接近“想要、追求奖赏”的行为驱动力,而不完全等于奖赏本身的快感体验。因此,动机并不只涉及是否获得愉悦,也涉及机体是否会持续朝某个目标投入行为。
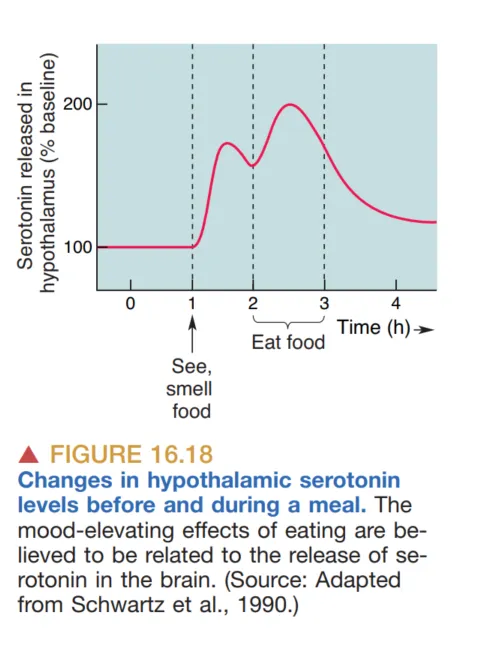
5.3 Serotonin、食物与情绪
5-HT(Serotonin,五羟色胺) 构成“食物—情绪”之间的重要连接点:5-HT 来源于饮食中的 tryptophan(色氨酸),而色氨酸在血液中的水平会随饮食中碳水化合物的比例变化。由此,食物组成可能通过改变脑内 5-HT 相关过程而影响情绪。脑内 5-HT 调节异常也被认为与进食障碍有关,因此动机不仅是奖赏问题,也与情绪背景有关。
6. 其他动机行为:饮水与体温调节
6.1 饮水
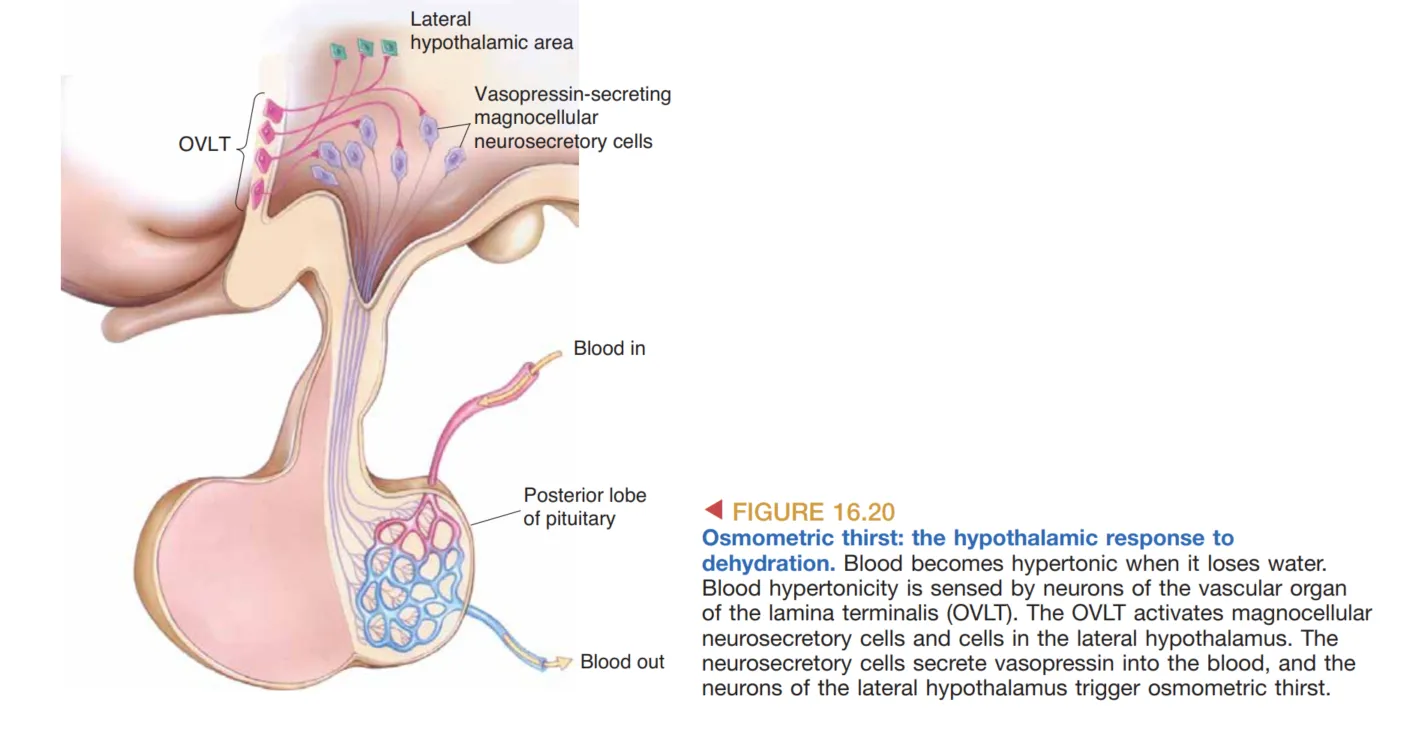
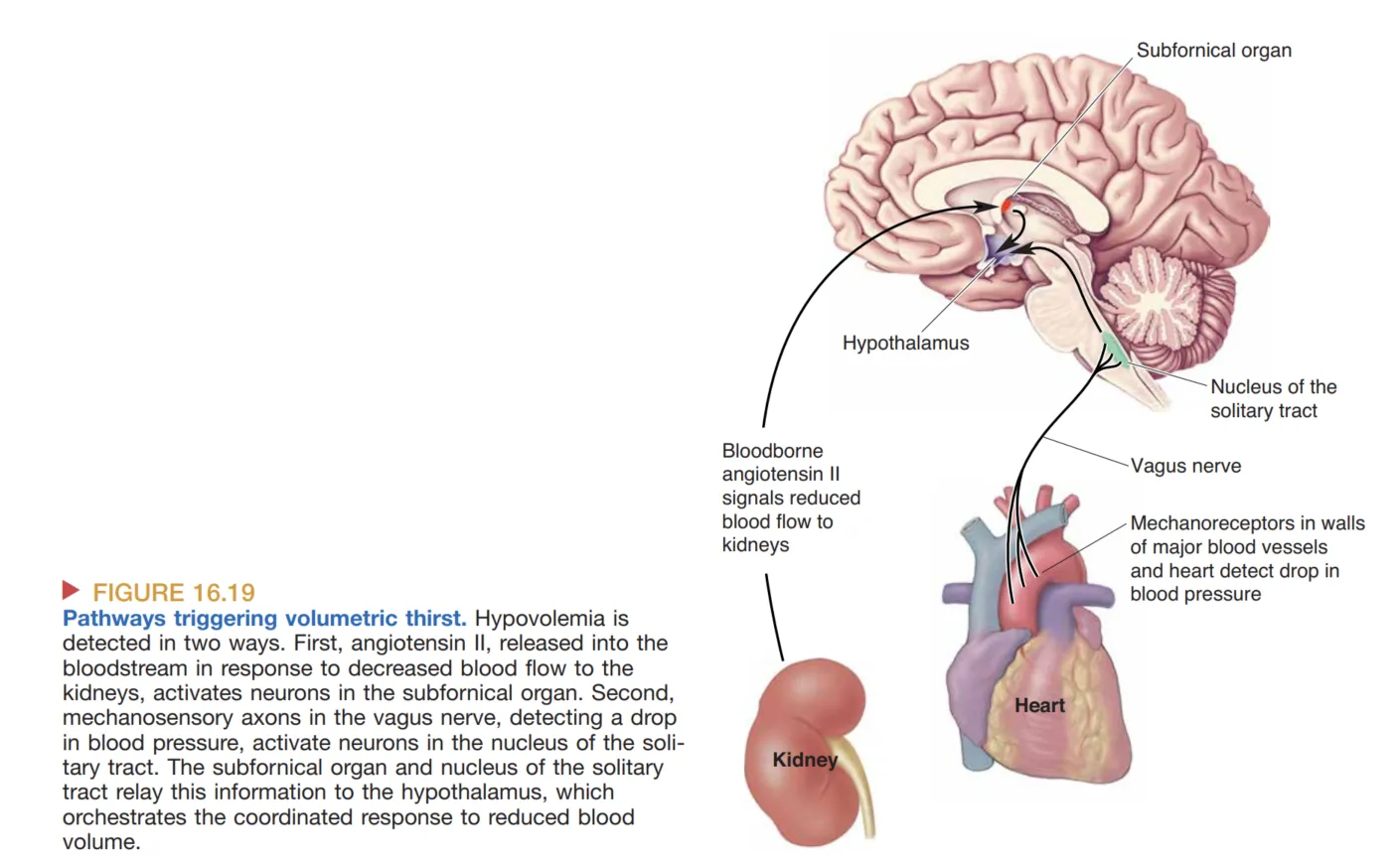 饮水行为可分为两种主要生理触发。第一类是 volumetric thirst(容量性口渴),与 hypovolemia(血容量不足) 有关。课堂补充指出,这一过程可通过肾素—血管紧张素系统激活 subfornical organ(穹窿下器),再引发下丘脑与 ADH(抗利尿激素) 相关反应。第二类是 osmometric thirst(渗透性口渴),与血液高渗相关;这类信号可由缺乏血脑屏障的 OVLT(血管终板器) 感受,并进一步驱动下丘脑反应。
饮水行为可分为两种主要生理触发。第一类是 volumetric thirst(容量性口渴),与 hypovolemia(血容量不足) 有关。课堂补充指出,这一过程可通过肾素—血管紧张素系统激活 subfornical organ(穹窿下器),再引发下丘脑与 ADH(抗利尿激素) 相关反应。第二类是 osmometric thirst(渗透性口渴),与血液高渗相关;这类信号可由缺乏血脑屏障的 OVLT(血管终板器) 感受,并进一步驱动下丘脑反应。
 这两类口渴说明,饮水行为并非来自统一的“主观想喝水”感受,而是来自不同生理偏差进入不同感受器与脑区后的汇聚输出。它们再次体现了下丘脑在动机中的通用角色:把内环境失衡翻译成行动。
这两类口渴说明,饮水行为并非来自统一的“主观想喝水”感受,而是来自不同生理偏差进入不同感受器与脑区后的汇聚输出。它们再次体现了下丘脑在动机中的通用角色:把内环境失衡翻译成行动。
6.2 体温
体温调节同样展示了下丘脑如何组织动机反应。体温升高由 anterior hypothalamus(下丘脑前部) 的 warm-sensitive neurons 检测,并伴随 TSH 释放减少;体温降低则由 cold-sensitive neurons 检测,并伴随相反变化。课堂补充进一步概括:体液与内脏运动反应更多由室周和内侧下丘脑组织,而行为行动则依赖外侧下丘脑。因此,寻找阴凉、靠近热源、减少或增加活动等行为,可以被理解为与激素和自主神经变化并列的一组纠偏输出。
Conclude
 该图对应“Hypothalamic Responses to Stimuli That Motivate Behavior”,用于概括饮水、体温等不同动机行为所涉及的下丘脑反应。
该图对应“Hypothalamic Responses to Stimuli That Motivate Behavior”,用于概括饮水、体温等不同动机行为所涉及的下丘脑反应。
